
部門紹介研究
INTRODUCTION OF
THE RESEARCH DEPARTMENT
開発候補品は、複数の創薬研究ステージを経て創出されます。その各ステージにおいて、様々な専門性を持つメンバーがそれぞれの役割をもって活躍しています。
(以下の図をクリックすると、それぞれのステージにおける仕事と役割をご覧いただけます)
アステラスの研究体制や研究活動についてはこちらをご覧ください

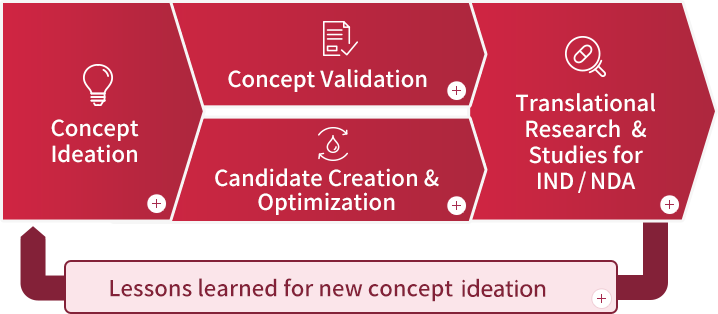
・IND: Investigational New Drug
・NDA: New Drug Application

Concept Ideation
創薬アイディアを精緻化し、創薬コンセプトを創り上げていくところから創薬研究が始まります。
生体分子や生理機序など、疾患関連性の高いバイオロジーに注目し、文献調査や種々データベースなどを駆使し、創薬標的を見極めていきます。
概要
新しい「くすりの種」を探す研究です
すでに多くの疾患に対する治療薬が開発・上市されていますが、いまだに満足な治療薬がない疾患も数多く存在します。また、すでに治療薬がある疾患でも、有効性が十分でない、副作用が強いなどの理由から、新しい治療薬が強く求められている疾患もあります。
Concept Ideationのステージでは、こうした疾患に苦しむ患者さんたちに革新的な医薬品を届けるために、疾患の背景にある個体レベル、細胞レベル、分子レベルでの変化から、病気や症状の原因を推定し、それを基に病態を改善する方法 (創薬コンセプト) を立案・検証しています。
創薬コンセプトの立案は、自社での研究結果だけでなくアカデミアをはじめとした他機関との共同研究からの知見、外部機関からの報告などを基に行います。また、立案した創薬コンセプトは化合物や抗体、核酸などのツールを用いて、個体レベルや細胞レベルで疾患に対する有効性を検証します。
病態モデルや細胞で効果が認められた創薬コンセプトは、Candidate Creation & Optimizationのステージに進み、医薬品として開発する形態 (低分子化合物、抗体、核酸、細胞など) に形を変えて、最適化研究が進められます。

Concept Validation
創薬コンセプトの確からしさを確認する研究です。
創薬コンセプトに基づき、求める生体反応や生理機能の評価方法を確立し、また目的とする有効性・安全性プロファイルを有する開発候補品を絞り込むための、適切なスクリーニングカスケードを作ります。
社員Q&A
 薬理研究職
薬理研究職薬学部 薬科学科卒
宮之原 遵 さん
現在の業務の役割や業務内容を
教えてください
Candidate Creation & Optimizationにおけるスクリーニングを経て選別された候補品の創薬コンセプトを、非臨床レベルで実証する役割を担っています。
既存薬や競合品では届けることのできない新しい価値を患者さんに提供可能であることを示す、説得力を持ったデータセットとストーリーの構築が求められる仕事です。
候補品が病態モデルで有効性を示すことはもちろんですが、同時にその作用機序を可能な限り明らかにすることが重要です。このValidationには、大きく3つの戦略的意義があると考えています。
1つ目は、競合優位性です。証明した作用機序から、既存薬や競合品に対してどのような付加価値があるのかを理論的に説明できるようになります。
2つ目は、安全性です。専門家と連携しながら進める安全性試験において何らかの毒性所見が認められた場合に、作用機序とは独立した回避可能な毒性であるか否かなどを考察するのに役立ちます。
3つ目は、患者層別化です。想定される作用機序は、どのような患者層を狙うべきかの議論の土台となります。この過程ではTranslational
Researchの一環で、例えば患者さんの検体を用いた薬理試験により、ヒトでの薬効が期待されるかを非臨床で検証することも少なくありません。
どのようなやりがい、
面白さや難しさがありますか
初期創薬終盤のテーマを担う立場として様々な関係者との連携が生じる中、特にグローバルな場で自分の考えを正しく伝えることに難しさを感じることが多いです。例えば海外の開発やコマーシャルなどの機能とは隔週で会議を行っておりますが、決して得意ではない資料準備や英語での対話に苦労しています。
それでも、自分なりに考え抜いたメッセージをぶつけて議論することではじめて、チームの目線が合ったと感じたり、新たな課題や必要な行動が浮かんできたりすることがあります。チームビルディングやテーマ推進に貢献できていると感じた瞬間は大きなやりがいを覚えます。
また、薬理研究者として日々新しい科学やデータに触れることができる環境にとても有難さを感じています。仮説通りの作用機序で強力な有効性を動物モデルで示したときのインパクトは忘れられません。科学への知的欲求と専門性を世の中の価値に変換できるのが創薬研究職の醍醐味だと考えています。
社員Q&A
 非臨床安全性研究職
非臨床安全性研究職医学部・保健学科 検査技術科学専攻卒
森 華奈子 さん
現在の業務の役割や業務内容を
教えてください
創薬コンセプトの立案後に、非臨床安全性の専門家として患者さんの安全性に影響する可能性がある科学的根拠を、早期に提示する役割を担っています。
アステラスは、最先端の科学で創薬を実現します。最も重要なのは、治療法が先進的かどうかではなく、患者さんに治療を受けて良かったと感じて頂くことです。そのためには、有効性だけでなく安全性にも配慮することが不可欠です。
16世紀の医師・化学者パラケルスス「すべてのものは毒であり、毒でないものはない。用量だけが毒でないことを決める」の言葉は毒性学の本質をよく表しており、安全性研究者はすべての生体反応とその用量を精査する研究を行い、薬理作用や薬物動態など様々な視点から得られた結果を総合的に解釈します。私はリスクとベネフィットの最適なバランスを見極めるプロファイラーです。
創薬プロセスの初期段階では、プロジェクトの成功に大きく影響する重要な安全性プロファイルを見極める研究を行います。複数の候補品から薬の種を選抜するカスケードの立案には、新しい科学技術を活用した安全性評価系の構築も不可欠です。創薬のスピードは非常に速いため、その流れを先読みし、最適な評価を行うことが求められます。
どのようなやりがい、
面白さや難しさがありますか
安全性プロファイリングには様々な専門知識を必要とし、すべてに精通することも大切ですが、実際には専門家で構成されるチーム活動が重要です。その中で、メンバーがどのように自分の専門性を発揮するかが、個々の腕の見せ所だと思います。毒性分野の専門知識を駆使し、最先端の技術を用いて新しい評価系を開発するケースも少なくありません。
一方で、創薬初期段階では時間や資金といったリソースが限られているのが現実です。また、近年では動物における3Rs※が社会的課題として注目されています。創薬は自社における課題だけでなく社会的課題も念頭において研究する必要があり、安全性の評価戦略をどのようにデザインするかに悩む時もありますが、同時に科学技術の革新を推進する大きなチャンスとも考えています。
私は生殖発生毒性の専門家として、動物実験に依存しない新しい研究に取り組んでいます。この研究はコンソーシアム研究として成果を公表し(こちらもご参照ください)、安全性を示すための新たな規制枠組みを提案するための基盤研究となりました。新たな評価手法を開発・導入することで、より効果的かつ信頼性の高い安全性評価を実現し、創薬プロセスをさらに進化させることを目指しています。
※3Rs; Refinement, Reduction, Replacement
森 華奈子さんの一日のスケジュール
| 8:30 |
通勤、出社 私の一日は、朝のメール、チャット、社内のSNSや掲示板の確認から始まります。社内では複数のコミュニケーションツールで情報交換が可能になり、場面や目的に応じて使い分けをしています。 |
| 9:00 | 実験開始 私の研究テーマは生殖発生毒性で、実験日には何よりも受精卵・胚の発生過程に沿って実験を進めることを優先します。 |
| 10:00 | 受精卵の様子を観察しつつ、メール確認などのデスクワークも並行して行います。 |
| 11:00 | 採材できる個数を確認し、実験が計画通りに実施可能かどうか判断し、午後の準備をします。 |
| 12:00 | 昼食 実験が忙しい日は急いで昼食を済ませることもありますが、居室のすぐ横にある食堂を利用し、同僚と他愛のない話をする完全オフ時間を楽しんでいます。 |
| 13:00 |
実験 実験は通常9時から15時に行います。その間、メールなどはタイムリーに対応できない場合があります。ただし、実験や会議の予定はすべて同僚と共有しているため、応答できない際も作業に集中しやすい環境です。 |
| 15:00 | 実験終了:データまとめ、試験立案 |
| 16:00 | 社内会議やデスクワーク 会議だけでなく、締め切りが迫る業務や研究のアイデア出しに取り組む場合も、それらに集中する時間を一日のスケジュールに組み込んでいます。 |
| 18:00 | 片付け、退社 フリーアドレスのため毎日デスクに何も置かず、片付けてから退社。片付けが苦手な方もすぐ慣れますよ! |
| 19:00 | 仕事終わりは週に1-2回、アステラスバドミントン部の練習に参加します。業務以外のコミュニティを持つこともできます。 |
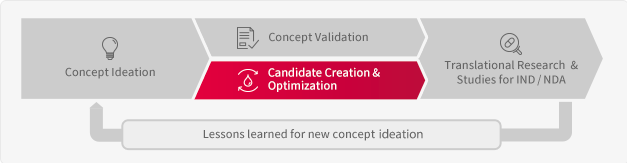
Candidate Creation & Optimization
開発候補品をデザインし、最適化する研究です。
プロトタイプの物質をスクリーニングもしくは収集した情報を基にデザインし、その後改変・修飾していくことにより開発候補品へ最適化していきます。
近年のAI技術の進歩、ロボットやコンピュータの性能の飛躍的向上は、創薬プロセスにも大きな影響を及ぼしています。蓄積された評価データを活用したAI・機械学習は効率的な開発候補品のデザインを可能にし、ロボットやコンピュータは効率的な評価と分析を可能にします。
社員Q&A
 バイオロジクス研究職
バイオロジクス研究職薬学部・薬学科卒
山﨑 莉佳 さん
現在の業務の役割や業務内容を
教えてください
主に、抗体創薬における「くすりの種」を探索し、それを最適化することで、開発候補品そのものを創製する役割を担っています。
アステラスは、細胞医薬や標的タンパク質分解誘導剤のような複数種の創薬モダリティを有しています。この強みを生かして、通常の抗体創薬に加え、他のモダリティと掛け合わせた改変抗体創薬にも取り組んでいます。具体的な研究業務として、期待するプロファイルを有する抗体取得に向けたスクリーニング系の構築、動物免疫等による抗体の取得、抗体活性評価のためのin
vitroやin vivo実験、AI・機械学習を活用したin silico抗体設計基盤構築などに取り組みます。
同時に、抗体創薬の専門家として、創薬研究プロセスの様々なステージにも携わります。例えば、テーマ創出にも携わりますし、コンセプト検証に必要な分子をデザイン・提供することで、創薬コンセプトの妥当性判断に貢献します。Translational
Research & Studies or IND/NDAステージのプロジェクトに参画し、開発候補品の非臨床試験を担う人もいます。
どのようなやりがい、
面白さや難しさがありますか
私は自分の分子設計によって「タンパク質」を、期待する薬効や物性を示す「バイオロジクス」に磨き上げることにやりがいを感じています。開発候補品そのものの構造を設計する仕事なので、新規治療法を待ち望んでいる患者さんに新薬を届けるための重要な業務に携わっていると感じ、モチベーションが高まります。
プロトタイプのタンパク質が最初から理想的な性質を持つことはほとんどありません。そのため、実験データや文献情報をもとに、DMTA(Design-Make-Test-Analyze)サイクルを何度も回しながら分子の最適化を進めます。
私の専門はタンパク質科学であり、タンパク質の作製や評価には自信がありますが、入社当初、薬としての薬効や物性などのプロファイル改善は未経験でした。それでも、「分子設計に挑戦したい」という熱意を評価いただき、ある研究テーマで候補分子のプロファイル改善を担当しました。経験豊富な研究員にフィードバックを求めながら設計案を詰め、自身の強みを生かして改変体の調製から評価を進めました。一度は基準を満たす分子を創出できたと思ったものの、新規に構築した高次評価系での評価結果を受けて再設計が必要になるなど困難もありました。しかし、データに真摯に向き合いながら粘り強く検討を繰り返した結果、最終的には良好なプロファイルを持つ分子を創出できたことが自信に繋がりました。
社員Q&A
 薬理研究職
薬理研究職生命理工学部 生命工学科 生命情報専攻卒
山下 恵里 さん
現在の業務の役割や業務内容を
教えてください
このステージでは、Concept Ideationのステージで新しく見つかった"くすりの種"から医薬品にふさわしいプロファイルに磨き上げられた開発候補品を見出す役割を担っています。
くすりの種は、薬力学的にも薬物動態的にも物性的にも、まだ荒削りの状態です。最終的に患者さんに投与されることをイメージしながら、より効きやすくより安全な開発候補品になるように最適化していきます。薬理担当者の業務としては、Concept
Validationで得た知見をもとにしたスクリーニングの実施や、適応疾患のバイオロジーを反映した病態モデルにおける薬効評価などが挙げられます。得られた評価結果を、薬物動態・メドケム・安全性などのスペシャリストたちとともに考察し、次の候補品のデザインに活かします。このように合成、評価、考察、次の合成とサイクルを回し続け、低分子化合物であれば合計何千もの化合物を合成・評価し、その中からたった1つの開発候補品を選び抜くことになります。
どのようなやりがい、
面白さや難しさがありますか
このステージの仕事の面白さはいたるところにあります。例えば、日々評価する候補品の中にとびぬけた薬効を示すものがあったとき。病態モデルでの薬効を予見できるよりよいスクリーニング系を構築できたとき。得られたデータをもとにチームで次の作戦を練っているとき…。そしてそういった一歩一歩を積み重ねた先にある開発候補品そのものを、自分たちの手で創出できるところにやりがいを感じています。私は「大好きな研究を通して社会の役に立ちたい」という気持ちがあってこの仕事を選びました。研究の成果物が社会に還元され、世界中の患者さんを救うイメージを持ちながら日々取り組んでいます。
もちろんその過程では最適化が想定通りに進まないことも多々ありますし、スクリーニングの系自体にトラブルが起きることもあります。決してルーチンワークなどではなく、観察眼や改善志向が求められる業務だと思います。
山下 恵里さんの一日のスケジュール
在宅勤務も含めた日のスケジュール
| 8:00 (出社) | 病態モデル作成/実験 | 出 社 |
| 11:00 (出社) | 新規テーマに関する会議 | |
| 12:00 | 午後は在宅勤務のため帰宅、休憩 | |
| 13:30 (在宅勤務) | 会議の議事録作成 | 在 宅 勤 務 |
| 14:00 (在宅勤務) | 取得した実験データの解析 | |
| 15:00 (在宅勤務) | 担当テーマの担当者会議 | |
| 17:00 (在宅勤務) | 派遣社員への業務依頼、実験ワークシートの準備 | |
| 18:00 (在宅勤務) | 業務終了 | |
出社日のスケジュール
| 8:30 (出社) | 被験物質の薬理試験 | 出 社 |
| 11:30 (出社) | 休憩 | |
| 12:30 (出社) | 被験物質の薬理試験 | |
| 14:30 (出社) | データ解析、資料作成など | |
| 17:00 (出社) | 薬理担当者内での相談 | |
| 17:30 (出社) | 業務終了 |
社員Q&A
 トランスレーショナルリサーチ/薬物動態研究職
トランスレーショナルリサーチ/薬物動態研究職医学薬学府 総合薬品科学専攻卒
山中 陽介 さん
現在の業務の役割や業務内容を
教えてください
開発候補品の最適化研究において、薬物動態の観点から新薬の原石を磨き上げる役割を担っています。
薬物動態研究とは、薬物が体内でどのように吸収、分布、代謝、排泄されるかを評価する研究です。薬理や安全性は薬物が生体に与える影響を評価するのに対し、薬物動態は薬物が生体から受ける影響を時間的、定量的に評価します。標的組織での薬物濃度を基に薬効のコンセプトを裏付けるとともに、適切な投与量や投与方法を決定します。また、薬物代謝酵素の同定や阻害能のデータを用いて、ヒトにおける薬物間相互作用のリスクを予測します。生成する代謝物のデータを基に、安全性試験における適切な動物種の選定やヒトにおける副作用リスクの低減に貢献しています。さらに、薬効を裏付けるバイオマーカーのデータを活用し、薬物動態(PK)と薬効(PD)の相関を解析します。これにより、種差を考慮したうえで、ヒトにおける最適な投与量や投与方法を予測します。Quantitative
Systems Pharmacology(QSP)やMicrophysiological
Systems(MPS)などの先進的な手法も取り入れ、予測精度の向上にも取り組んでいます。これらの評価を通じて、ヒトでの副作用を最小限に抑え、薬効を最大化できる開発候補品の選定に貢献しています。選定された開発候補品はTranslational
Research & Studies for IND/NDAのステージに進み、そのプロファイルをより詳細に解析し、理解を深めていきます。
どのようなやりがい、
面白さや難しさがありますか
従来型の低分子化合物の場合、薬物動態評価に関する方法論はある程度確立されており、得られたデータから薬理作用や副作用を理解し、ヒトでの予測も可能になってきました。一方、最近では医薬品として開発する形態(モダリティ)は、抗体、ウイルス、細胞、核酸など多様化してきています。このような新しいモダリティには従来の方法論が通用せず、また医薬品業界的にも知識やノウハウが不足しているため、私たちはゼロから評価方針を考える想像力と、それを着実に遂行する実行力が求められます。これらのモダリティでは、標的因子に関するバイオロジーに加えて薬理や安全性のデータが薬物動態を考えるうえで重要な手掛かりとなることも多く、合成、薬理、安全性、薬物動態の垣根を超えた協働が不可欠です。それぞれの課題に対してチーム全員で解決する意識が高く、ディスカッションを繰り返しながら課題を解決することができています。経験のない分野でゼロから方針を立て、未知の課題をチーム一丸となって乗り越えられる、大きなやりがいが得られる仕事です。私たちと共に、新しい挑戦に取り組んでみませんか?
山中陽介さんの一日のスケジュール
| 8:00 | 海外との会議(試験で得られたデータについてのディスカッション、方針策定など) |
| 9:00 | 通勤 |
| 10:00 | 出社(フリーアドレスのオフィスのため)仕事準備 業務開始、メール確認、対応 |
| 11:00 | 社内会議 |
| 12:00 | 昼食 |
| 13:00 | 社内会議 |
| 14:00 | 試験データの確認、考察、ディスカッション、資料作成 |
| 15:00 | 社外委託試験の担当者と打合せ |
| 15:30 | 試験データの確認、考察、ディスカッション、資料作成 |
| 17:00 | (在宅勤務の場合)学童保育へ子供のお迎え |
| 17:30 | 試験立案 |
| 19:00 | 片付け、退社 |
社員Q&A
 メディシナルケミスト職
メディシナルケミスト職薬学系研究科・薬科学専攻卒 薛 贇唯 さん
薬学部・薬学研究科卒 今出 慧海 さん
現在の業務の役割や業務内容を
教えてください
薛さん:
メディシナルケミストとして、新薬候補分子の設計・合成・評価および分析(DMTA;
Design-Make-Test-Analyze)サイクルを推進することです。このステージは新薬創出の核心に位置し、非常に重要な役割を果たしています。
Concept Ideationのステージで得られた標的情報や初期データをもとにDMTAサイクルを回し、最終的に最適化された開発候補品をTranslational Research & Studies
for IND/NDAのステージに引き渡します。パラレル合成を実施しつつ複数のテーマを同時に担当することもあります。このステージの効率化は、創薬プロセス全体の課題でもあります。
近年、AIとロボット技術は大きく発展しています。私たちのチームではこれらの技術を活用したプラットフォームを構築し、このステージの期間を短縮させています。具体的には、AIを用いた化合物構造の設計や生成、反応条件の最適化、物理化学的性質や薬物動態特性の予測など、多岐にわたる機能を活用しています。また、AIと連携したロボット合成機の導入により、多数の反応を効率的に進行させるだけでなく、取得したデータを基にした構造活性相関(SAR)解析やAI予測との比較分析も可能となりました。これにより、開発候補品の取得までの時間短縮を目指しています。
今出さん:
同じく、メディシナルケミストとして新たな開発候補品の創出におけるモノ作りの役割を担っています。疾患関連性の高いバイオロジーを起点として創薬コンセプトに合致する適切なモダリティを設定します。所属するエンジニアードスモールモレキュールズ(ESM)においては特に分解誘導剤を中心としたモダリティを扱っています。起点となる化合物の取得方法を検討し、取得した化合物の見極めとその後の分子構造の最適化を実施しています。化合物を最適化する際には構造生物の活用や、薬効・安全性への関連性の高いパラメータの理解が重要になります。近年は抗体-薬物複合体の応用も進めており、より複雑な分子構造の化合物を生み出すため高い技術力が求められます。
物性、動態、安全性を担保した開発候補品の創製は、次のステージへと進めるためのマイルストーンの一つです。また前臨床試験実施のための化合物供給、さらに臨床試験のための化合物製造に向けた研究も開発候補品が絞られてきた早い段階から検討していくことで、より確からしい戦略立案へとつなげることができます。
さらに、創薬コンセプトの検証に対して、検証に資する化合物を提供することもあります。どのようにコンセプトを証明していくか評価を進める中で得られた知見を元に議論しプロジェクトを推進していきます。
どのようなやりがい、
面白さや難しさがありますか
薛さん:
このステージにおける最大のやりがいは、自ら設計・合成した化合物がin vitroやin
vivoの実験で薬効を示し、最終的に患者さんの治療に貢献できる可能性が見えた瞬間です。設計図上の分子構造がAI技術などと融合した化学手法により、効率的な合成、評価、分析を経て開発候補品として形になる過程は、メディシナルケミストとして非常に充実感を感じます。また、医薬品研究の最前線で日々新しい知識やアイデアに触れられる点も大きな魅力です。
一方、このステージでは多くの挑戦にも直面します。例えば、設計した分子の活性と構造の相関性が期待通りの結果を示さないことも多く、その原因を究明するためには専門知識の深さと柔軟な発想が求められます。特に、近年ではモダリティの多様化によりAIの予測が適用しづらいケースもあり、予測精度を向上させるには、モデルに適切なデータを継続的に供給することが必要です。さらに、複数の研究テーマ(海外からもあります!)を並行して進めるためには、効率的なスケジュール管理とチーム間の円滑なコミュニケーションが欠かせません。
今出さん:
開発候補品ひいては医薬品になりうるものを自らの手でデザインできるところにやりがいを感じています。研究に携わっている化合物が医薬品として患者さんの元に届き、健康や治療に役立っていることをイメージして仕事に取り組んでいます。
研究では起点となる化合物のタネをどのようにとってくるのか、さらに化合物をブラッシュアップしていく過程に科学的な楽しさがあります。サイエンスとして世の中で未知の発見が得られた時はミステリーを解いたような面白さがあります。またone
Astellasとしてプロフェッショナル同士がチームとして医薬品という目標に向かって進んでいけるところは楽しく、海外拠点の同僚との交流も新たな視点が得られる機会になります。
疾患の治療には魅力的であるものの制御が困難なターゲットをいかに制御するかが目下の課題です。これらを制御できるモダリティやノウハウが求められています。そのためアステラスの中での知見の蓄積とともに、常にグローバルな科学の進歩には目を光らせながら研究に取り組んでいます。科学の進歩を医薬品に繋げる、日々この挑戦に立ち向かっています。
薛 贇唯さんの一日のスケジュール
| 8:30 | 出社、メール確認、当日のタスク整理 |
| 9:00 | AIのサポートによる分子デザイン、新規合成方針の立案 |
| 10:00 | 化合物の合成実験(場合により 手合成/パラレル合成/ロボット合成) |
| 12:00 | 昼食、昼休憩 |
| 13:00 | 井戸端会議または部門間連携会議(進捗報告、安全衛生確認、情報共有および次の合成方針検討) |
| 14:00 | 合成した化合物の物性分析結果の確認(LC-MS、NMRなど) |
| 14:30 | 合成実験の結果確認、後処理、精製および分析依頼 |
| 16:30 | バイオチームから提供された化合物の活性データをAIに提供して分析を行い、次の分子設計へ反映 |
| 17:30 | 翌日の準備 |
| 18:00 | 退社 |

Translational Research & Studies or IND/NDA
開発候補品の臨床効果の指標を探索したり、ヒトに投与しても安全かどうかを確認する研究です。
得られた開発候補品の有効性や安全性、体内動態など、開発候補品のプロファイルをより詳しく調べます。また、臨床試験や医薬品承認申請に向けた戦略策定や、規制要件を満たすために必要な研究、承認取得後の販売促進に寄与するための研究も行います。
社員Q&A
 非臨床安全性研究職
非臨床安全性研究職農学部 資源生物科学科卒
木上 大輔 さん
現在の業務の役割や業務内容を
教えてください
臨床試験へ進める開発候補品の選択において、安全性の観点から情報を提供する役割を担っています。
そして、臨床試験が開始されたあとも、安全性研究は続けられ、第1相から3相、新薬の承認申請に至るまで、各ステージで必要とされる情報を提供していきます。
具体的には、
臨床試験の開始:臨床試験開始前には、医薬品ガイドラインに沿って開発候補品の安全性試験を行い、得られた情報から、臨床での副作用のリスクマネジメントプランへ繋げています。
承認申請まで:新薬を患者さんへ届けるため、その価値を明確にする必要があり、有効性と安全性のリスクベネフィットを示すことが大切です。安全性研究は、このリスクを明らかにすることに貢献しています。
一方、Translational researchにおける安全性研究の役割は幅広く、創薬初期の研究も行います。創薬標的のオンターゲットや、標的以外のオフターゲットの安全性をin vitroやin
vivoのみならず、in silicoなど多角的に評価し、より質の高い候補品の選択に貢献しています。
どのようなやりがい、
面白さや難しさがありますか
私たちは治療薬のない領域に取り組み、遺伝子治療や細胞医療といった研究に挑戦しています。最先端の科学を取り入れ、安全性研究においても、遺伝子発現解析といった分子生物学的な視点からの評価も行っており、こういった新たな研究に興味をかきたてられ、アクティブな日々を過ごしています。そして、開発候補品が臨床試験を開始するステージまで進むと、米国や欧州の臨床開発メンバーとの協働が活発になり、グローバルに研究開発が展開されていきます。このグローバル開発のため、海外出張の機会もあり、現地のメンバーと会い、私は異文化コミュニケーションを楽しみました。
医薬品開発で最も大事なことは、何よりも、その治療薬を待ち望まれる患者さんに新薬を届けることです。私たちの研究活動が、患者さんのニーズに応えることができるという信念に基づいて研究に励み、やりがいを感じています。
このような最先端の創薬研究を行い、まだ見ぬ新薬を私たちと一緒に創っていきませんか! 皆様とお会いできることを楽しみにしております。
社員Q&A
 トランスレーショナルリサーチ/薬物動態研究職
トランスレーショナルリサーチ/薬物動態研究職畜産学部・獣医学科卒
佐山 裕行 さん
現在の業務の役割や業務内容を
教えてください
Translational Research(TR)は非臨床研究の成果を臨床に橋渡しする一連の研究を指しますが、その内容は多岐に渡ります。私たちはTRの目的を「臨床開発におけるProof of
Conceptの成功確率を上げること」と捉えて研究活動を進めています。
私たちのTRの一例として、開発候補品の薬効を臨床試験で確認するバイオマーカーの探索やヒト組織サンプルを用いた薬効・安全性の検証などが挙げられます。私が担当している数理モデル(こちらもご参照ください)を用いた解析もTRの活動の一部です。Concept
Validationのステージでは、様々な実験で候補品の作用仮説が検証されます。私たちはそこで得られたデータを数理モデルで解析することでその定量的な理解度を高めます。また、構築した数理モデルにヒトとの種差に関する情報を組み入れることにより、ヒトでの候補品プロファイルを予測し臨床試験デザインの策定にも貢献しています。数理モデル解析業務は、非臨床で得られた様々な知見を定量的に理解し、その理解に基づいて臨床を予測する、まさに橋渡し研究と言えます。
どのようなやりがい、
面白さや難しさがありますか
医薬品開発における数理モデル活用の歴史は古く、候補品の体内動態を表すPharmacokineticモデル、体内動態と薬理効果指標の関係性を表すPharmacokinetic-Pharmacodynamicモデルなどが活用されてきました。近年ではQuantitative Systems Pharmacology(QSP)モデルという新しい数理モデルが注目されており私たちも力を入れています。QSPモデルは病気の仕組みそのものをモデル化し、薬物の作用と生体反応の複雑な相互作用を解析します。そのため解析者には高度なモデル構築技術に加えて、バイオロジーの深い理解が求められます。これはとても難しいことですが、薬理研究者と協働してモデルを作り上げていく過程はとてもやりがいを感じますし、構築したモデルでバッチリデータを再現できたときは心躍ります。そのように構築されたQSPモデルは臨床でも様々な目的で活用されます。最近は特に自社候補品と市販薬との併用薬理効果を予測して臨床試験計画をサポートすることに力を入れており、実際の臨床開発の現場に貢献できることには面白さを感じますし、とてもやりがいのある仕事です。
社員Q&A
 薬理研究職
薬理研究職薬学部薬学科卒
沼崎 真子 さん
現在の業務の役割や業務内容を
教えてください
治験薬申請や新薬承認申請に必要な薬理試験のストーリーや戦略の策定ならびにそれら薬理試験の信頼性確保と大きく2つの役割を担っています。
Candidate Creation &
Optimizationステージで選ばれた開発候補品は、次に臨床試験(治験)において、実際にボランティアさんや患者さんに投与し、安全性や有効性を評価することになります。治験を開始するためには、各国の規制当局に臨床試験開始申請(IND)が必要です。また、治験で有用な結果が得られた開発品は上市に向けて、医薬品承認申請(NDA)をする必要があります。
Translational Research & Studies or IND/NDAステージでは、Candidate Creation &
Optimizationステージの研究者と連携し、申請に必要な薬理試験のストーリーや戦略を策定し、信頼性の高い薬理試験報告書を作成します。社内だけでなく、CROや共同研究などの社外リソースを活用して試験報告書を作成することもあります。また、承認取得後の販売促進に寄与するための研究を行うこともあります。一方、非臨床薬理試験の信頼性を確保することも重要です。信頼性確保のための運用システムやルールの最適化をするとともに、品質保証部との連携や、研究者への信頼性教育など、試験計画策定から報告書作成までの非臨床薬理試験全般に関するコンサルテーションを行っています。
どのようなやりがい、
面白さや難しさがありますか
医薬品承認申請を控えた業務は、非常に刺激的で緊張感のある業務の1つです。新薬が患者さんのもとに届くまでのカウントダウンが始まるこの時期は、日々の業務に正確性と迅速性が求められますが、業務の一つ一つが患者さんの未来に直結しているという実感があり、責任とやりがいを感じることができます。承認申請や当局対応は、製薬企業ならでは業務であり、研究とはまた違った視点を学ぶことができるのも大きな魅力です。
国内外問わず、さまざまなプロジェクトに関与することで、最先端の科学に触れる機会が増え、知識の幅を広げる機会が多いことも、この業務の魅力の1つです。互いの専門性を持ち寄って、チームで結束して、まだない薬を世の中に提案できることは非常にやりがいがあります。
非臨床薬理試験において、何よりも重要なことは信頼性の確保です。既存のルールを遵守するだけでなく、信頼性確保のための運用システムやルールを最適化するために、世界各地の研究拠点のメンバーと意見交換することは、さまざまな視点を学び合う貴重な機会でもあります。また、製薬各社との意見交換も、貴重な機会です。

Lessons learned for new concept ideation
臨床試験において有効性・安全性が明らかになり、患者さんへの価値が規制当局から認められれば医薬品が上市されていきます。一方で、臨床試験で明らかになった知見をもとに、さらに新しい医薬品創生のアイディアが生まれてくることもあります。製薬企業ではこのサイクルを継続的に続けることで、患者さんに継続的に価値を提供していきます。前臨床研究と臨床試験でのアウトカムの相関に対する理解を深める研究も行います。
勤務地
-
つくば研究センター(茨城県)
アクセスマップ






